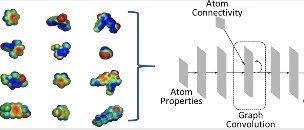
静电势表面
众所周知,分子的静电性质可以用于预测分子的化学反应性及分子间相互作用力。一般来说,分子ESP表面是通过在分子表面上移动单位电荷探针生成的。在分子表面上的每个点处,计算探针的ESP能量,然后对分子表面进行着色。在药物研发中,静电相互作用力的优化至关重要。而ESP表面在很大程度上取决于基础静电模型的质量。由于多种原因,蛋白质-配体相互作用的静电很复杂。这些效应只能通过量子力学(QM)计算来准确地捕获,但计算量很大,因而无法将其用作常规的药物设计的工具。

构建训练集和测试集
为了推导并验证小分子ESP表面相关的图卷积DNN模型,作者构建了一个训练集以及测试集。训练集分子选自eMolecules和Sigma-Aldrich中可购买化合物的数据集,最大程度地覆盖化学空间,HAC≤17且仅由元素B,Br,C,Cl,F,H,I,N,O,P和S组成的分子,总数100500。从ChEMBL中构建测试集,总数4815。对于这两套数据,作者都确保了广泛的化学空间范围以及与药物化学的相关性。对于测试集以及数据集中的每一个分子:首先通过DFT计算分子的电子密度,生成分子表面,根据DFT电子密度和电子核的位置计算出分子表面上的ESP值,以创建DFT-fp模型。

图1. 训练集以及测试集上的验证
图片来源JMC
深度神经网络模型结果
针对训练集生成的DFT-fp对DNN模型进行了训练。 上图显示了DFT-fp Δq值相对于训练集的预测DNN-fp值的曲线图。 显然,该模型能够很好地描述训练集分子的点电荷,R2 = 0.996,RMSE Δq= 0.010e。 此外,在整个训练集中RMSEV平均值为3.30 kcal / mol,DNN-fp 模型生成的ESP表面质量近似于DFT-fp计算出的ESP表面。 将DNN-fp模型在测试集中的表现,显示DNN-fp和DFT-fpΔq值之间具有良好的相关性,其中R2 = 0.981,RMSE Δq= 0.022e。
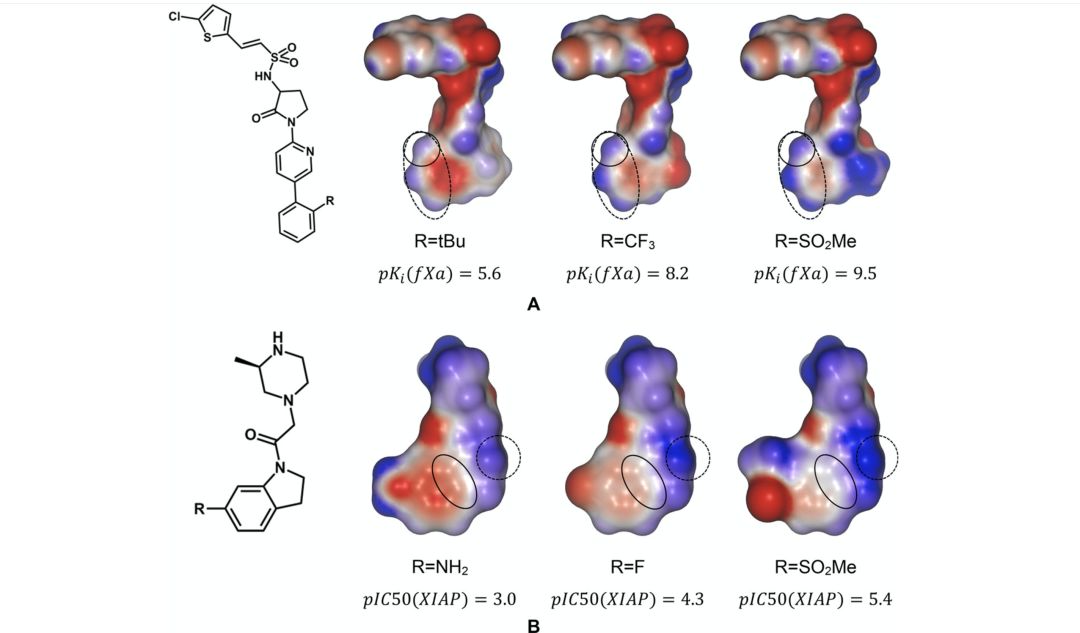
图2. 通过DNN-fp模型生成的ESP表面积
图片来源JMC
总结
作者开发出一种快速生成高质量的ESP表面的方法。对于小分子,作者使用100 000多种分子训练了图卷积DNN模型。结果表明该DNN模型与DFT方法所建立的ESP表面具有良好的一致性。 并且,DNN-fp模型可在不到一秒钟的时间内生成ESP表面,完全可以将其用于药物设计。对于蛋白质,作者开发了一种快速生成ESP表面的方法,后续的实验表明,DNN-fp ESP表面与与分子实际的理化性质之间存在很强的相关性。
参考文献
Practical High-Quality Electrostatic Potential Surfaces for Drug Discovery Using a Graph-Convolutional Deep Neural Network. Prakash Chandra Rathi, R. Frederick Ludlow, and Marcel L. Verdonk. Journal of Medicinal Chemistry Article ASAP, DOI: 10.1021/acs.jmedchem.9b01129