
先睹为快
作者
日本千叶大学药学系Hajime Sato教授
日本东京大学药学系Masanobu Uchiyama教授
研究对象
巴西烷型天然产物trichobrasilenol的生物合成途径
计算方法
密度泛函理论(DFT)
计算软件
GRRM11, Gaussian 16
计算细节
所有计算均采用基于Gaussian 16程序的GRRM11。结构优化在气相下M06-2X/6-31+G(d,p)水平上进行;并在同一水平上计算振动频率,以检查每个优化结构是能量最小点(无虚频率)还是过渡态(单一虚频率);通过内禀反应坐标(IRC)追踪过渡结构到相应的局部极小值的最小能量路径(MEP);在M06-2X优化结构的基础上,计算mPW1PW91 /6-31+G(d,p)水平下的单点能量;本文讨论的吉布斯自由能是通过加入气相吉布斯自由能修正来计算的;最终的羟基化反应,采用自洽反应场(SC RF)方法,采用极化连续介质模型(PCM)对溶剂化进行了评价。
巴西烷型倍(Brasilane-type)半萜类化合物的研究由来已久,但其生物合成途径和机制尚不清楚。最近,有课题组鉴定了一种木霉萜环化酶,该酶能催化产生巴西烷型倍半萜- trichobrasilenol,并利用同位素标记法研究该天然产物形成的机理,然而,在所提出的机理中,高度协同的骨架重排的可行性备受争议。本文作者结合AFIR方法与DFT计算探究了trichobrasilenol(具有巴西烷型倍半萜的骨架)生物合成途径中所有可能反应机制,提出了一种新的非常规骨架重排机制,涉及一个多步碳阳离子级联,其中cyclopropylcarbinyl阳离子与homoallyl阳离子平衡起关键作用。这一途径和机理与以往有关巴西烷类化合物及相关萜类化合物的生物合成研究(包括同位素标记实验和副产物分析)是一致的。
研究内容
巴西烷型结构具有双环[4.3.0]壬烷骨架,常出现在倍半萜类化合物中,但其生物合成途径和机制目前还不清楚。近期,有两个课题组分别鉴定了一种萜烯环化酶,该酶催化法尼基焦磷酸(FPP)形成巴西烷型骨架产物trichobrasilenol。Kuzuyama等人并利用同位素标记法研究该天然产物形成的机理(图1)。在所提出的机理中,以5/7/3三环中间体为原料,通过复杂的协同反应,包括C−C σ键的置换和重排、环收缩、π键形成和区域选择性羟基化等六个化学事件,最后合成巴西烷5/6双环骨架;然而在所提出的机理中,高度协同的骨架重排的可行性备受争议,并且无法解释水分子只在C8位发生反应。因此,作者期望通过计算的手段来解析trichobrasilenol的生物合成机制。
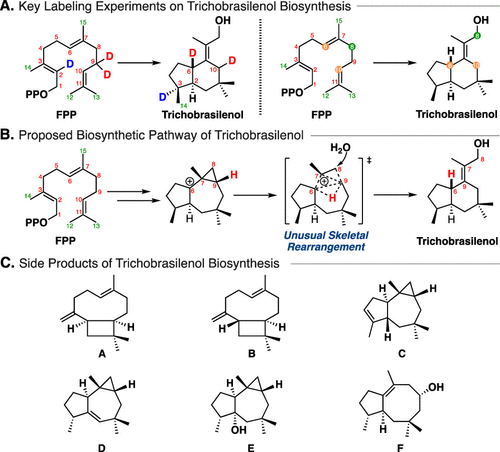
图1. Trichobrasilenol生物合成的前期研究内容
图片来源于:JACS
尽管量子化学计算在方法上取得了进展,但对于复杂化学反应的理论研究仍然存在挑战,主要是因为这些反应涉及广泛的键重排,存在许多可能的相关路径,以往对这种复杂反应的理论研究大多只考察根据直觉和经验选择的少数几种途径。作者认为提出一个合理的生物合成途径,有必要考虑可能的相关途径,包括各种碳阳离子的作用以及键和骨架的重排。2013年Keiji Morokuma教授与Keiji Morokuma教授共同开发了一种,
图2展示了FPP转化为中间体IM8的最有利途径以及与IM1有关的相对能量。反应开始于FPP焦磷酸盐的解离,产生一个烯丙基阳离子中间体IM1,通过阳离子-π与远端C10−C11双键作用稳定。事实上,C11(+0.37 au)的自然居群分析(NPA)正电荷相比烯丙基阳离子(C1−C2−C3)更高。因此,阳离子介导的环化过程可以顺利进行,形成所谓的humulyl阳离子中间体IM2,经过1,2-H迁徙,得到第一个较稳定的homoallyl阳离子(IM3)。从IM3中NPA电荷分布可以看出,homoallyl阳离子与相应的cyclopropylcarbinyl阳离子处于平衡状态,其中高度扭曲的环丙烷C−C键有效地稳定了相邻的碳正离子,因此,尽管IM3是二级C+离子,但它出人意料地稳定。接着经过一个cyclopropylcarbinyl阳离子过渡态(TS_3-4)形成5/7/3三环中间体IM4。随后,连续两次的1,2-H迁徙,历经一个IM5中间,形成最稳定的三级碳阳离子IM6。中间IM6b包含一个高度扭曲的环丙环,其中拉长的C7−C9 σ轨道的参与有助于相邻C6碳正离子的稳定。接着,经历一个非常规骨架重排和环收缩过渡态TS b−7a,能垒为16.6 kcal/ mol,得到5/6双环中间体(IM7a)。IM7a具有双环[4.3.0]壬烷骨架,IM7a经历很小的活化势垒形成另一个环构象的IM7d,接着发生了1,2-H迁徙,得到了能量上更稳定的烯丙基碳阳离子IM8。最后,在C8位发生SN2′型水合反应,生成最终产物trichobrasilenol。但目前还不清楚最后的水合步骤是在酶的内部还是外部进行的。
作者对中间体IM7a做了进一步的IRC(内禀性反应坐标)计算(图3)。结果表明这一步包括三个化学过程:(i)从5/7/3到5/6/4三环系统的骨架重排,形成环丁基叔碳阳离子(shoulder_b−7a),(ii)C8−C9 σ键断裂和C7−C9 π键的形成产生homoallyl阳离子(TS_6b−7a),以及(iii)异丙烯基(shoulder2_6b−7a)通过1,2-迁徙得到另一个homoallyl阳离子(IM7a)。通过追踪C6−C7−C8−C9上的键长和NPA电荷变化,结果与碳正离子重排过程一致。
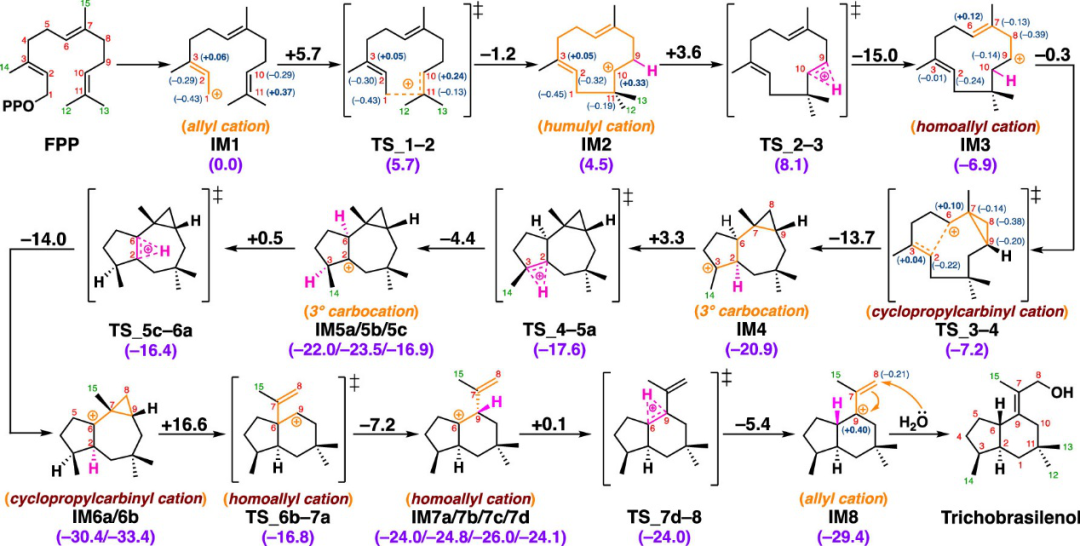
图2. Trichobrasilenol生物合成全过程的DFT计算结果
图片来源于:JACS
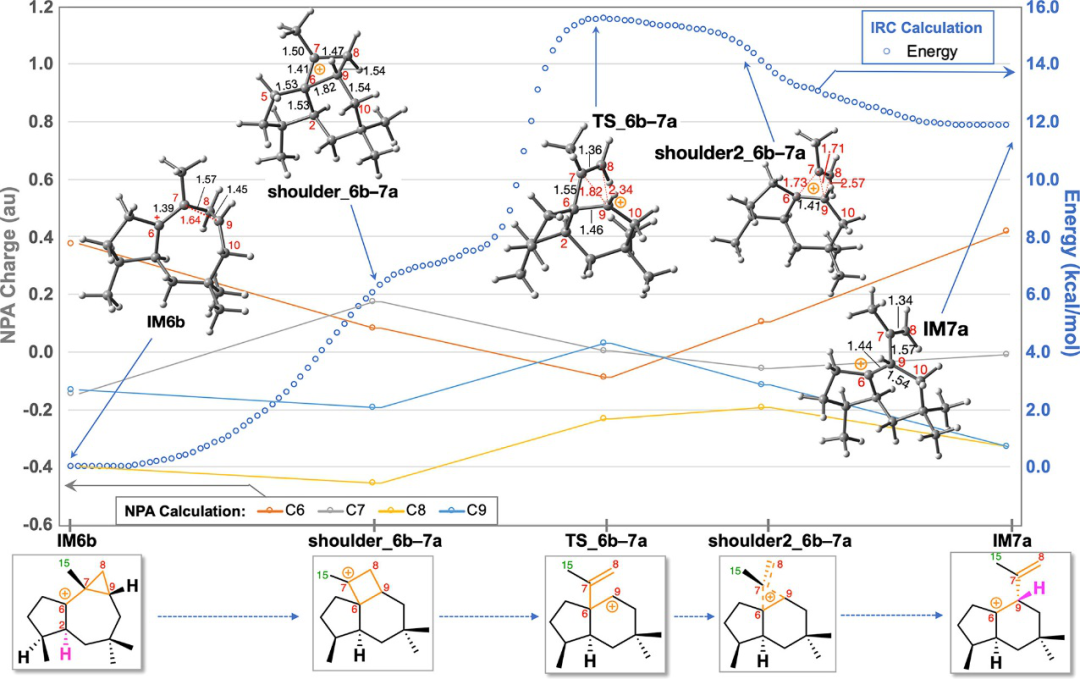
图3. IM6b向IM7a转化过程中键长和NPA电荷变化及IRC结果
图片来源于:JACS
结果与讨论
综上所述,作者通过分子、原子和电子尺度上的计算研究揭示了trichobrasilenol生物合成的反应途径和机理(图4)。从全局自由能曲线来看,整个反应在动力学(能垒没有超过20kcal/mol)及热力学上都是有利的(放出热量约30kcal/mol),其中限速步鄹(能垒:16.6 kcal/mol)发生在(IM6b → TS_6b−7a)的非常规骨架重排(图3),包括了三个过程:(i) 从5/7/3到5/6/4三环的骨架重排,(ii)σ键断裂,(iii)异丙烯基的1,2-迁徙。新提出的催化机制成功地解释其他萜烯和萜类化合物的形成。特别是,这项工作强调了cyclopropylcarbinyl阳离子和homoallyl阳离子的平衡关系在催化过程的重要性,可以作为萜烯生物合成的中间产物。
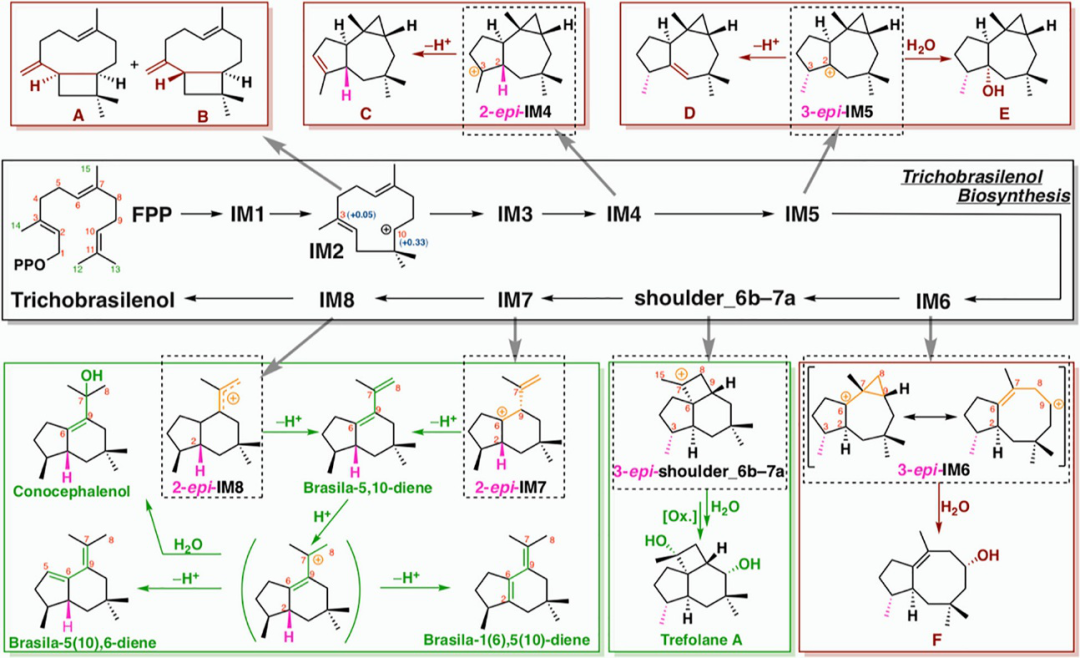
图4. 基于计算提出的Trichobrasileno及相关副产物A−F生物合成途径
图片来源于:JACS
参考文献
Hajime Sato, et al. DFT Study of a Missing Piece in Brasilane-Type Structure Biosynthesis: An Unusual Skeletal Rearrangement. J. Am. Chem. Soc. 2020, 142, 47, 19830–19834, DOI: 10.1021/jacs.0c09616