
引言
手性醇是大量复杂化合物的重要组成部分,在制药、农业化学、香味和精细化工行业发挥重要作用。利用脱氢/还原酶对前手性酮进行不对称生物还原是制备手性醇的重要方法。然而工业有广泛应用的非天然底物,天然酶具有催化活性有限或立体选择性不足的问题。本文通过分子动力学模拟发现影响催化的关键氨基酸,然后进行定向突变重新设计,得到突变酶大大提高了手性醇的转化率。
先睹为快
单位与作者
福州大学(Juan Lin)与浙江大学(Li-Dan Ye, Hong-Wei Yu)
计算方法与模型
Mu0及其突变体的同源性模型基于NADH依赖的1-(4-羟苯基)-乙醇脱氢酶的晶体(PDB ID: 4URF), PpYSDR及其突变体用铜绿假单胞菌 PAO1的羰基还原酶(PDB ID: 5WQO)
计算软件
分子对接AutoDock 4,分子动力学模拟(Amber 18)
计算亮点
基于限制性分子动力学(MD)模拟中酶与底物复合物构象变化,作者提出了一种基于对MD模拟中有/无底物的酶/底物结合模式分析的策略,即有距离限制(预反应状态)模拟和无距离限制自由状态模拟。以对庞大的芳基酮活性较差的短链脱氢酶/还原酶(SDR)突变体EbSDR8-G94A/S153L(Mu0)为例,将模拟中构象差异明显的H145和Y188作为目标,作者重建了底物结合口袋,同时调节了C1和C2口袋相对大小来提高立体选择性,以此方式设计了用于有效不对称还原邻卤代苯乙酮,丙苯酮,芳族酮酸酯和二芳基酮的突变体,从而将手性醇的转化率提升到大于 99%,ee提高到大于 98%。通过分子模拟表明,找到合适的结合口袋能改善提高对不同结构的底物的活性和立体选择性,这是普遍存在的机制。这项研究为合理设计具有宽底物谱和高立体选择性的醇脱氢酶/还原酶提供了更多的策略。
研究结果
Kazlauskas规则广泛用于预测和改善酯酶和脂肪酶的立体异构构象结构。因此,在T-state和free-state状态比较分析和Prelog规则的指导下,对Mu0重新进行了设计,用于不对称还原各种前手性酮(图1)。设计原理和策略随后被用于对PpYSDR的结构修饰,进行验证。
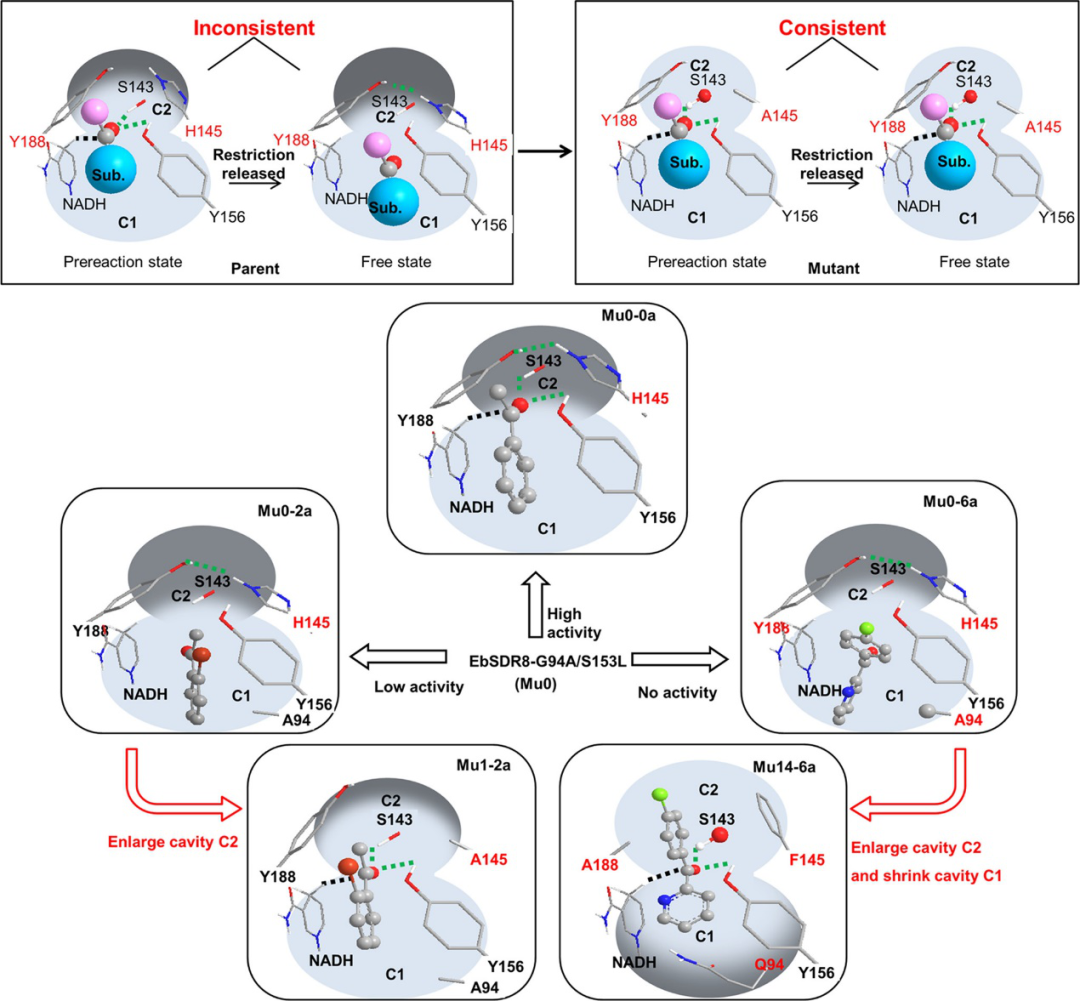
图1. EbSDR8-G94A/S153L (Mu0)的重新设计
图片来源 ACS Catalysis
在计算模拟中预反应状态(Prereaction-State)可用于预测酶对底物的反应性。在脱氢/还原酶的情况下,当催化酪氨酸的羟基氧(OH)与底物(Osub)的羰基氧形成氢键,同时NAD(P)H的C4N处的氢原子与底物(Csub)的羰基碳足够接近能转移氰化物时,预反应状态形成。因此,通过计算构象中O sub和OH Y156之间距离[d(Osub-OHY156)] ≤2.8 Å和Csub跟H18NADH之间距离[d(Csub -H18NADH)] ≤3.0 Å的占有率来确定预反应状态形成的可能性。
为了计算形成预反应状态的概率,作者将Mu0和难还原酮组装成Mu0-2aProR用于分子对接,随后分别进行了两个状态的分子模拟(T-state和free-state)。选择最低能量的结构代表每个模拟中的结合模式。模拟结果表明两种模拟之间结合方式的明显差异,暗示难以形成预反应状态。一方面d(Osub-OH1Y156) 和d(Csub-H18NADH) 在F-state模拟中分别达到 4.24和4.68 Å, 另一方面,同时满足d(Osub-OH1Y156) ≤ 2.8 Å和d(Csub-H18NADH) ≤ 3.0 Å 的催化构象比例为0(图2A),显示出难以完成质子和氢化物转移的过程。
作者发现发现残基H145和Y188通过彼此靠近,形成氢键的可能性很高(d(OHY188-NE2H145) ≤ 3.2 Å 的比率达到25%) ,T-state和free-state状态模拟后的结合模式明显不同(图2B),free-state状态的模拟中发现不适当的能量分布(图3 E),形成了称为Mu0-6aProR的R手性醇,因此,H145和Y188被确定为改造的目标残基。作者随后将H145和Y188替换为较小的残基(分别为丙氨酸,甘氨酸和半胱氨酸),几乎所有测试的底物的转化率均得到了不同程度的提高(图3)。
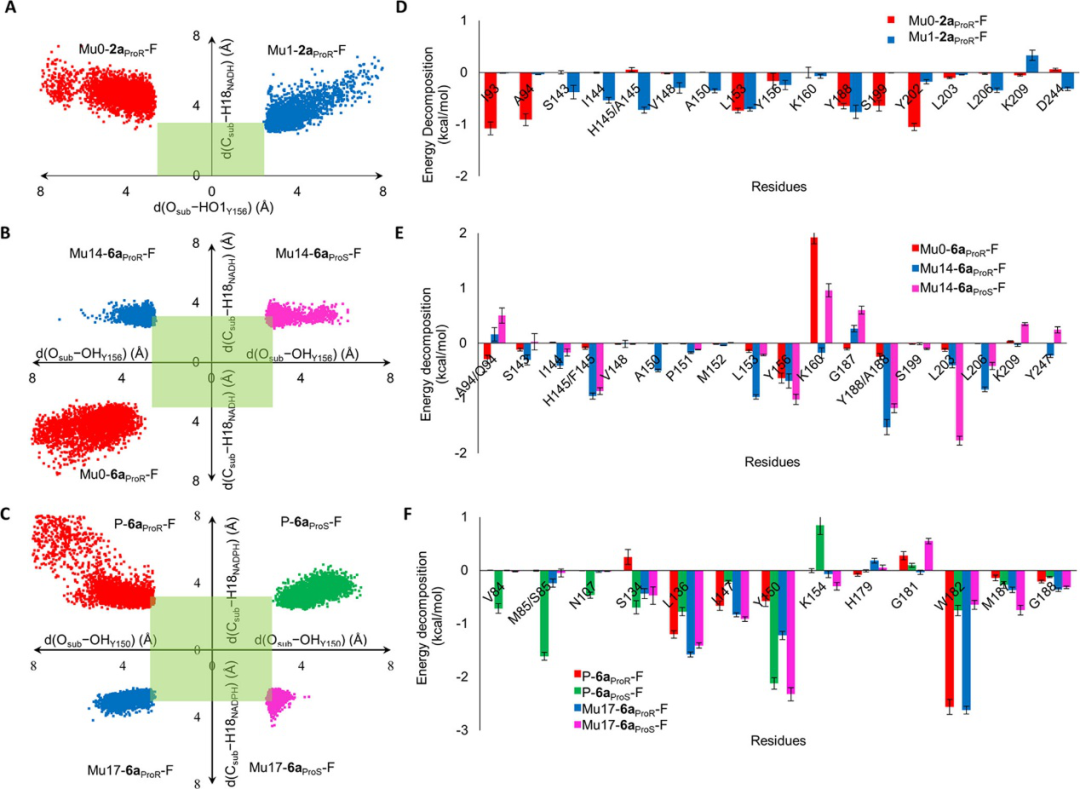
图2. Free-state状态时,底物结合袋中残基的构象分布图和能量分解
图片来源 ACS Catalysis
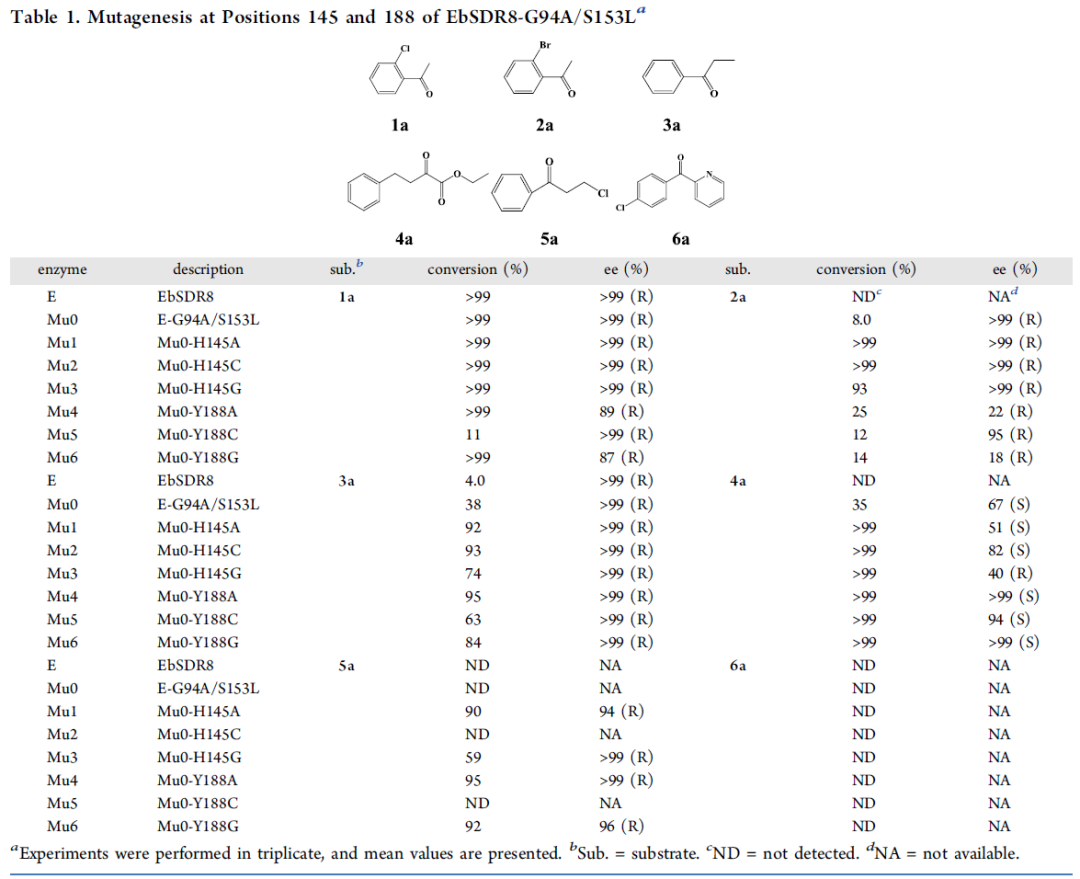
图3. 突变酶的转化效率
图片来源 ACS Catalysis
参考文献
Rational Design of Dehydrogenase/Reductases Based on Comparative Structural Analysis of Prereaction-State and Free-State Simulations for Efficient Asymmetric Reduction of Bulky Aryl Ketones Bing-Mei Su, Ze-Hui Shao, Ai-Peng Li, Muhammad Naeem, Juan Lin, Li-Dan Ye, and Hong-Wei Yu. ACS Catal. 2020, 10, 864−876. DOI: 10.1021/acscatal.9b04778